Small Struct |上海藥物所合作構建遞送納米粒的納米網格新載體
文章來源:上海藥物研究所 | 發(fā)布時間:2024-02-03 | 【打印】 【關閉】
脂質體、外泌體等納米制劑在疾病治療領域已有廣泛應用��,但仍存在體內停留時間短��、清除速率快等挑戰(zhàn)�����,合適的遞送載體可改善其體內行為�,達到更好的治療效果�。關于藥物分子的遞送研究已持續(xù)幾十年,而對于納米粒遞送的研究卻極少�����,且分子水平的治療劑適用的載體通常無法遞送納米粒�����。所以��,制備生物安全����、具有開放孔道�����、孔徑在納米尺度范圍的多孔載體����,用于納米粒的遞送�����,將為藥物遞送開辟新思路�����。
2024年1月30日�����,中國科學院上海藥物研究所張繼穩(wěn)團隊與沈陽藥科大學王淑君團隊聯(lián)合在Small Structures上發(fā)表了題為“Supramolecular Nano-Grid Platform to Load and Deliver Liposomes and Exosomes”的研究論文�����。該研究以環(huán)糊精為基本結構單元�����,構建了一種新型的納米網格結構載體,其不僅具有pH/H2O2雙響應性�����,還能通過多孔網狀的納米結構負載脂質體和外泌體:將脂質體靶向遞送到肺部并延長其體內作用時間���,實現(xiàn)外泌體遞送并達到長時間釋放效果����。
研究人員基于環(huán)糊精金屬有機骨架的有序結構����,針對環(huán)糊精單元上不同位點的羥基活性差異��,采用對稱型硼酸酯鍵交聯(lián)劑����,對其進行交聯(lián),通過控制反應條件����,得到納米網格狀和球形兩種不同結構特征的硼化有機骨架(BOF)。其中���,納米網格狀結構由數(shù)十納米直徑的纖維交織而成�,分布有10-300 nm的開放空間。硼酸酯鍵交聯(lián)劑賦予BOF以pH/H2O2雙響應性����,其在生理pH環(huán)境下穩(wěn)定、在炎癥或腫瘤內環(huán)境下迅速降解�����,在pH 7.4時的半衰期是pH 5.0的467倍����,H2O2存在時降解速率顯著加快。
納米網格結構和球狀結構的BOF
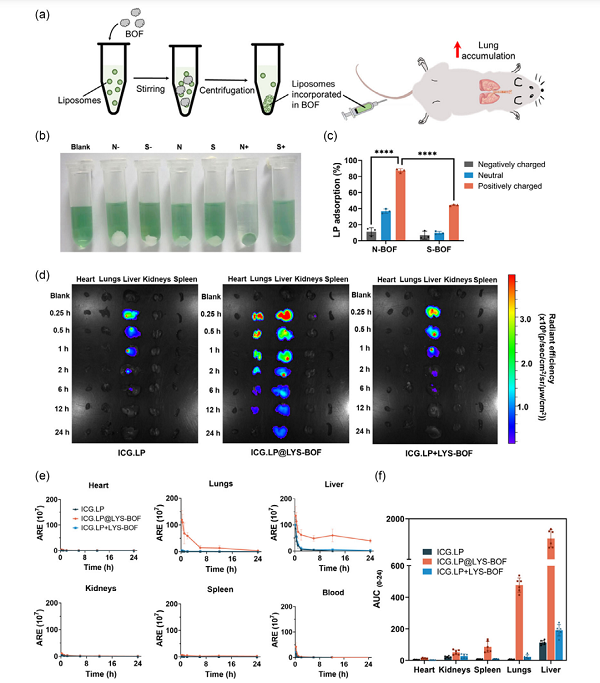
研究表明�����,納米網格狀結構的BOF(N-BOF)比球狀BOF(S-BOF)具有更好的脂質體俘獲效果��,并能顯著改變脂質體在小鼠體內的生物分布:游離脂質體在肺部幾乎沒有分布����,負載于N-BOF后,脂質體在肺部的熒光信號顯著增強,肺部生物利用度提高約90倍�����。
N-BOF的脂質體負載能力及對脂質體生物分布的影響
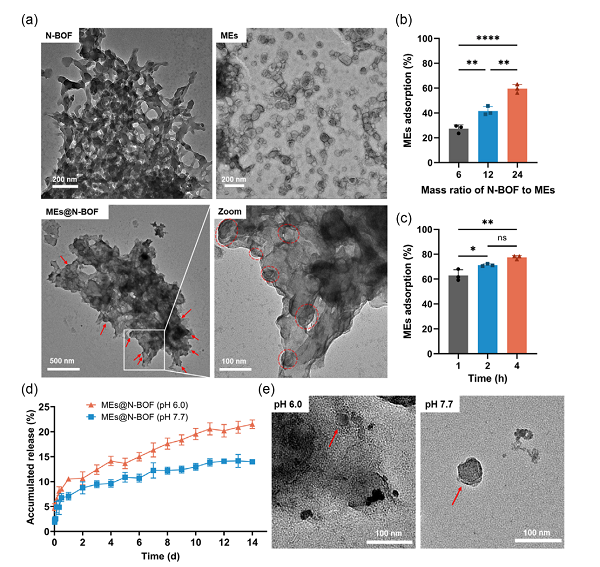
牛奶外泌體的粒徑為50-150 nm����,處于N-BOF孔徑的主要分布范圍內。N-BOF對牛奶外泌體具有良好的俘獲效果�����,利用透射電鏡可以觀察到脂質雙層結構的外泌體分布在N-BOF顆粒上���。N-BOF能夠響應性釋放所負載的外泌體��,在pH 7.7環(huán)境中,14天內N-BOF對外泌體的釋放量為14%��,而pH 6.0環(huán)境下釋放量則為21%��,且釋放出的外泌體仍能保持完整的結構�����。
N-BOF對牛奶外泌體的俘獲及pH響應性釋放
上海藥物所碩士研究生李晶為本文第一作者,上海藥物所碩士研究生馬武珍進行了外泌體部分的研究����,沈陽藥科大學博士研究生楊伯陽完成脂質體制備。上海藥物所張繼穩(wěn)研究員��、伍麗副研究員和沈陽藥科大學王淑君教授為本文共同通訊作者�����。該研究得到了國家自然科學基金和國家重點研發(fā)計劃等項目的資助��。